ОПЫТ ПРИМЕНЕНИЯ ГИДРОГЕЛЯ ИЗ ПУПОВИНЫ ЧЕЛОВЕКА В ЛЕЧЕНИИ ПОСТРАДАВШИХ С ГЛУБОКИМИ ПОВРЕЖДЕНИЯМИ МЯГКИХ ТКАНЕЙ И КОЖИ
ОПЫТ ПРИМЕНЕНИЯ ГИДРОГЕЛЯ ИЗ ПУПОВИНЫ ЧЕЛОВЕКА В ЛЕЧЕНИИ ПОСТРАДАВШИХ С ГЛУБОКИМИ ПОВРЕЖДЕНИЯМИ МЯГКИХ ТКАНЕЙ И КОЖИ
журнал "Клиническая патофизиология" № 4 2024г.
Цель – клиническая оценка эффективности тканеинженерного гидрогеля из пуповины человека в лечении двух пациентов с объемными дефектами мягких тканей нижних конечностей.
Запатентованная технология изготовления гидрогеля из пуповины человека состояла в удалении ядер и клеточного дебриса детергентным методом, а получение солюбилизированной формы гидрогеля – ферментативным путем с последующей лиофилизацией и финишной стерилизацией.
Гидрогель из пуповины человека применяли в лечении двух пациентов с объемными повреждениями мягких тканей и кожи как дополнение к аутодермотрансплантации, так и самостоятельно. Гидрогель активно адсорбировал экссудат, ускорял формирование струпа, появление грануляций и эпителизацию, не вызывал лихорадочных и воспалительных реакций.
Представленные клинические наблюдения демонстрируют возможность успешного заживления глубоких и обширных ран с помощью лиофилизованного гидрогеля из Вартонова студня пуповины человека.
Ключевые слова: обширный дефект мягких тканей, расщепленный аутодермотрансплантат, несвободный суральный лоскут голени, гидрогель, пуповина человека, тканевая инженерия
EXPERIENCE OF HUMAN UMBILICAL CORD HYDROGEL USING IN THE TREATMENT OF PATIENTS WITH SOFT TISSUES AND SKIN DEEP INJURIES
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
S.M. Kirov Military medical academy, St. Petersburg, Russian Federation
The aim is to evaluate clinically the effectiveness of tissue–engineered hydrogel from the human umbilical cord in the treatment of two patients with large defects of the soft tissues of the lower extremities.
The patented technology for manufacturing the human umbilical cord hydrogel consisted in removing nuclei and cellular debris by the detergent method, and fabricating a solubilized form of hydrogel by enzymatic means followed by lyophilization and final sterilization.
Human umbilical cord hydrogel has been used in the treatment of two patients with large soft tissue and skin injuries as an addition to autodermotransplantation, and independently. The hydrogel actively adsorbed exudate, accelerated scab formation, granulation and epithelialization, and did not cause feverish and inflammatory reactions.
The presented clinical observations demonstrate the possibility of successful healing of deep and extensive wounds using lyophilized hydrogel from Warton jelly of the human umbilical cord.
Keywords: extensive soft tissue damage, split autodermal graft, non-free sural shin flap, hydrogel, human umbilical cord, tissue engineering
ВВЕДЕНИЕ
Объемные дефекты мягких тканей требуют продолжительного многоэтапного лечения, и в этом смысле представляют собой самостоятельную проблему как гражданского, так и военного здравоохранения. Длительность лечения больших дефектов мягких тканей влечет за собой дополнительные значительные экономические затраты. При этом приемлемый результат достижим не всегда, в том числе из-за грубого рубцевания ран.
Появление продуктов тканевой инженерии показало их способность изменять процесс заживления с репарации на регенерацию благодаря структурным компонентам, факторам роста, молекулам клеточной адгезии, сохраняемым в природных пропорциях в тканеинженерных изделиях. Компоненты стимулируют такие гистогенетические процессы, как миграция, интеграция, пролиферация и дифференцировка собственных клеток реципиента, завершающиеся ремоделированием зоны дефекта. В ВМедА разработан и запатентован бесклеточный неиммуногенный гидрогель из высокорегенеративного биоматериала пуповины человека, отвечающего трансплантационным требованиям видовой совместимости, для лечения глубоких и обширных дефектов мягких тканей и кожи [1].
МАТЕРИАЛЫ И МЕТОДЫ
МАТЕРИАЛЫ И МЕТОДЫ
Клинические наблюдения в клинике военной травматологии и ортопедии ВМедА проведены с разрешения ЛЭК «Медицинские технологии» СФ_ЛЭК_МТ_07.02 от 06.06.2022г.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Рис.1
А - вид раны с медиальной поверхности голени
Б - вид с передней поверхности голени;
В- пластика дефекта несвободным лоскутом икроножной мышцы
Г- частичный некроз лоскута
Д –повторная трансплантация расщепленным кожным лоскутом, нанесение гидрогеля из пуповины
Е- аутотрансплантат без признаков воспаления и патологического отделяемого
Рис.2
Б - 18 день после ранения, аутодермопластика передне-наружной поверхности левой голени расщепленным дерматомным трансплантатом
В - применение гидрогеля из пуповины
Г – 21 сутки после аутодермопластики
Патофизиологической особенностью воспалительных процессов в зоне обширных и глубоких ран является выраженность явлений вторичной альтерации, еще больше увеличивающей зону повреждения тканей за счет деятельности лизосомальных ферментов, избытка протонов водорода, выделяемых разрушенными клетками. Микробное загрязнение при первичном повреждении и неоднократная хирургическая обработка для удаления некротизированных участков и инородных тел, проводимая на этапах оказания медицинской помощи, увеличивают объем повреждения. В огнестрельных ранах зона первичного поавреждения расширяется вторично за счет зоны молекулярного сотрясения; обилие инородных тел по ходу нелинейного раневого канала и микробное загрязнение провоцируют фагоцитарные эффекты иммунных клеток, что также увеличивает зону дефекта.
Оценки разными исследователями эффективности аутодермопластики как хирургической технологии ускоренного заживления при повреждениях кожи и мягких тканей расходятся в зависимости от причины повреждений, локализации (верхние или нижние конечности), сочетания аутодермопластик на конечностях и иных других областях тела, времени, прошедшего до момента оказания специализированной помощи, и ряда иных факторов. Для травматических повреждений пластика несвободным лоскутом эффективна в первые дни с момента повреждения [2]. При ранней тангенциальной некрэктомии у тяжелообожженных отмечена высокая эффективность кожной пластики (86,4%) в области верхних конечностей. В группе пациентов, хирургическое вмешательство которым было выполнено на нижних конечностях, показатель эффективности имел меньшие значения –75,9% [3]. Hashmi с соавт. (2023) показали, что из 49 случаев только в 35 (71,6%) случаях травм лодыжек и стоп наблюдалось полное заживление латерального супрамаллеолярного лоскута без осложнений [4]. Таджимуратовым с соавторами среди 146 пересадок кожи для закрытия обширных травматических дефектов кожи и мягких тканей полное приживление аутотрансплантатов отмечено после 124 (84,9%) операций, хорошее и удовлетворительное после 14 (9,6%) и полный лизис трансплантатов наблюдался после 8 (5,5%) операций [5].
Таким образом, возможности закрытия обширных и глубоких дефектов аутотрансплантатами ограничены и в 15-25 % случаев аутодермопластика неэффективна. Поэтому поиск и разработка новых средств и медицинских изделий, способных оптимизировать процессы приживления аутотрасплантатов и заживления ран, своевременны.
Гидрогель из пуповины человека представляет собой пористую легкую сыпучую порошкоподобную массу, содержащую полипептиды, несульфатированные и несульфатированные гликозаминогликаны, фактор роста эндотелия сосудов, трансформирующий фактор роста-β3, фибронектин, остатки ДНК в количестве менее 50 нг/мкл и менее 200 пар оснований, и остаточные количества детергента, не превышающие порога цитотоксичности. Благодаря своему составу он способствует адгезии клеток реципиента, их функционированию, обеспечивающему со временем создание новой ткани, восполняющей утраты структуры в ране. В доклинических исследованиях на разных видах лабораторных животных (грызуны, зайцеобразные, свинья) лиофилизованный гидрогель из Вартонова студня пуповины человека проявил себя как безопасное эффективное неиммуногенное средство, стимулирующее регенерацию тканей в зоне дефекта мягких тканей и кожи [6].
Гидрогель из пуповины человека отвечает трансплантационным требованиям видовой совместимости с организмом реципиентов. Бесклеточность гидрогеля является, на наш взгляд, значимым достоинством изготовленного продукта, обеспечивая его неиммуногенность, а также позволяя сохранять его в незатратных условиях длительное время и удешевляя его изготовление. Лиофилизованная форма гидрогеля активно адсорбирует раневой экссудат в первые минуты применения и фиксируется в ране. Высушенный гидрогель сохраняет биоактивность после 1 года хранения, что привлекательно для военной медицины и гражданского здравоохранения [7].
ЗАКЛЮЧЕНИЕ
ЗАКЛЮЧЕНИЕ
ЛИТЕРАТУРА
ЛИТЕРАТУРА
2. Ткаченко М.В., Хоминец В.В., Иванов В.С., и др. Отдаленный результат лечения пациента с обширным циркулярным дефектом мягких тканей нижней трети голени: клинический случай. Травматология и ортопедия России. 2024;30(1):110-119. Doi.org/10.17816/2311-2905-17472
3. Зиновьев Е.В., Солошенко В.В., Костяков Д.В. и др. Возможности объективизации иссечения при ранней тангенциальной некрэктомии у тяжелообожженных - MEDLINE.RU (Медико-биологический информационный портал для специалистов). 2022;23:801-811.
4. Hashmi P.M., Kamran A.S, Ali M, et al. Supramalleolar Flap for Soft Tissue Coverage of Foot and Ankle Defects: Largest Case Series at a Tertiary Care Hospital. J Plast Surg Hand Surg. 2023;57(1-6):459-465.
5. Таджимуратов Н.К., Семенов В.Г., Жамашев Д.К. и др. Эффективность аутодермопластики при обширных травматических дефектах кожи и мягких тканей» Вестник
КазНМУ.2015;16317-318.
6. Kondratenko, A.A.; Tovpeko, D.V.; Volov, D.A. et al. Decellularized Umbilical Cord as a Scaffold to Support Healing of Full-Thickness Wounds. Biomimetics 2024;9(405):1-20. Doi.org/10.3390/ biomimetics9070405
7. Кондратенко А.А., Калюжная Л.И., Товпеко Д.В. и др. Биологические и функциональные свойства лиофилизированных форм тканеинженерных матриксов из пуповины человека. Вестник трансплантологии и искусственных органов. 2023;XXV(1):113-122. Doi: 10.15825/1995-1191-2023-1-113-122
ПОТЕНЦИАЛ НЕТКАНЫХ МАТЕРИАЛОВ ДЛЯ ВОССТАНОВЛЕНИЯ ПЕРФОРАЦИИ БАРАБАННОЙ ПЕРЕПОНКИ
ПОТЕНЦИАЛ НЕТКАНЫХ МАТЕРИАЛОВ ДЛЯ ВОССТАНОВЛЕНИЯ ПЕРФОРАЦИИ БАРАБАННОЙ ПЕРЕПОНКИ
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
1Военно-медицинская академия им. С. М. Кирова, г. Санкт-Петербург, Россия
2 Институт высокомолекулярных соединений РАН, Санкт-Петербург, Россия
журнал "Клиническая патофизиология" № 4 2024г.
Целью работы было изучить возможность применения скаффолда из нетканого материала, несущего аутологичные фибробласты для регенерации перфорации барабанной перепонки.
Материалы и методы: нетканый материал для тканеинженерной конструкции был получен методом электроспиннига из поли-L-лактида, аутологичные фибробласты выделены из биоптата кожи с холки морских свинок, жизнеспособность клеток на носителе подтверждена микроскопически путем окрашивания ядер адгезированных к волокнам носителя клеток флуоресцентным красителем; исследование эффективности тканеинженерной конструкции проводилось на морских свинках с моделированной перфорацией барабанной перепонки на правом и на левом ухе.
Результаты: проведенная через 3-4 недели отоскопия под микроскопом показала отсутствие перфорации в ухе, где была проведена имплантация материала с клетками, в другом ухе барабанная перепонка восстановилась не полностью; результаты гистологического исследования тканей барабанной перепонки показывают локализацию клеток фибробластной морфологии на срезе тканей барабанной перепонки, а также прорастание кровеносными сосудами, что говорит о регенерации тканей после имплантации, а также отсутствие фрагментов скаффолда, что говорит о резорбции нетканого материала за прошедшее время.
Заключение. Применение пористого нетканого материала из полилактида для закрытия перфорации барабанной перепонки является менее травматичным методом по сравнению с традиционными хирургическими методиками лечения перфорации барабанной перепонки. Время полного восстановления сопоставимо со временем самопроизвольного заживления. Использование нетканого носителя в сочетании с аутологичными фибробластами индуцирует формирование структуры барабанной перепонки. Полученные результаты могут быть использованы для расширенного исследования эффективности и безопасности нетканого материала из поли-L-лактида для лечения хронической перфорации барабанной перепонки.
Финансирование
Авторы заявляют об отсутствии внешнего финансирования при проведении исследования.
Ключевые слова: исследование на животных; нетканый материал; перфорация барабанной перепонки; полилактид; тимпанопластика; тканеинженерная конструкция; фибробласты
POTENTIAL OF NONWOVENS FOR REPAIRING TYMPANIC MEMBRANE PERFORATION
The purpose of the work was to study the possibility of using a scaffold made of nonwoven material carrying autologous fibroblasts for the regeneration of perforated tympanic membrane.
Materials and methods: nonwoven material for the tissue-engineered structure was obtained by electrospinning from poly-L-lactide, autologous fibroblasts were isolated from a skin biopsy from the withers of guinea pigs, the viability of cells on the carrier was confirmed microscopically by staining the nuclei of cells adhering to the fibers of the carrier with a fluorescent dye; A study of the effectiveness of the tissue-engineered design was carried out on guinea pigs with simulated perforation of the tympanic membrane on the right and left ears.
Results: otoscopy performed 3-4 weeks later under a microscope showed the absence of perforation in the ear where the material with cells was implanted; in the other ear, the eardrum was not fully restored; The results of a histological examination of the tympanic membrane tissue show the localization of cells of fibroblastic morphology on a section of the tympanic membrane tissue, as well as the sprouting blood vessels, which indicates tissue regeneration after implantation, as well as the absence of scaffold fragments, which indicates the resorption of the nonwoven material over time.
Conclusion. The use of porous nonwoven material made of polylactide to close the perforation of the eardrum is a less traumatic method compared to traditional surgical methods for treating perforation of the eardrum. The time for complete recovery is comparable to the time for spontaneous healing. The use of a nonwoven carrier in combination with autologous fibroblasts induces the formation of the tympanic membrane structure. The results obtained can be used for an expanded study of the effectiveness and safety of poly-L-lactide nonwoven material for the treatment of chronic eardrum perforation.
Funding
The authors declare that there was no external funding for the study.
Keywords: Animal Experimentation, fibroblasts, nonwoven material, poly(lactide), tissue-engineered construction, tympanic membrane perforation, tympanoplasty
АКТУАЛЬНОСТЬ
Рис.1
Распределение анатомической локализации травм ЛОР-органов во время военных конфликтов
Fig. 1.
Distribution of anatomical localization of injuries to the ENT organs during military conflicts
- наружный эпидермальный слой (кератиноциты);
- средний фиброзный слой (фибробласты и коллаген II и III типа);
- внутренний эпителиальный слой (плоский неороговевающий эпителий).
Барабанная перепонка не является однородной структурой, ее толщина варьирует от 30 до 150 мкм. Средний фиброзный слой определяет механические параметры барабанной перепонки, такие как упругость, эластичность, и как следствие – остроту слуха [3].
После травмы возникает дефект барабанной перепонки – перфорация, которая ведет к частичной или полной потере слуха. В большинстве случаев перфорации заживают спонтанно в течение 7-30 дней, но в 25-30 % случаев этого не происходит, перфорации, сохраняющиеся более трех месяцев, классифицируются как хронические. Клинически это может проявляться стойким снижением слуха, гнойными выделениями из уха, болью, головокружением и шумом.
Классический подход к пластическому закрытию стойких перфораций предполагает использование фрагментов собственных тканей пациента (хряща, фасции височной мышцы, перихондрия), но полного восстановления барабанной перепонки не получается из-за гистологического несоответствия этих тканей ткани барабанной перепонки. Результат зависит от многих факторов: тщательность деэпидермизации краев перфорации, толщины трансплантата, опыта хирурга владением микрохирургическими навыками. Положительный исход хирургического лечения составляет 75-90 %. Не исключены повторные перфорации перепонки [4]. Поиск новых подходов к лечению хронической перфорации является актуальной задачей.
Среди альтернативных подходов в настоящее время проводятся исследования с применением подходов тканевой инженерии. Регенерация барабанной перепонки отличается от регенерации других тканей отсутствием опоры для миграции эпителиальных клеток. Методы тканевой инженерии предполагают использование скаффолдов для регенерации. Скаффолды могут быть получены децеллюляризацией тканей (дермальный аллотрансплантат, ксенотрансплантат бычьего перикарда, подслизистая оболочка тонкого кишечника свиньи, трансплантат, децеллюляризированная стенка мочевого пузыря), что имеет ограничение с точки зрения безопасности и этических аспектов или созданы из биосовместимых полимеров [5].
Коммерчески доступными биоматериалами для закрытия перфорации БП являются коллаген, желатин, фиброин шелка, хитозан, целлюлоза, полидиметилсилоксан, полимолочная кислота (полилактид), поликапролактон, поли(этиленоксидтерефталата)/поли(бутилентерефталата) (ПЭОТ/ПБТ) гиалуроновая кислота и альгинат в меньшей степени.
Отмечено, что в экспериментальных исследованиях упоминается использование факторов роста для регенерации БП совместно со скаффолдом или как самостоятельное средство. Несмотря на показанную эффективность воздействия фактора роста фибробластов и эпидермального фактора роста, существуют осложнения при их использовании [6].
ЦЕЛЬ ИССЛЕДОВАНИЯ
МАТЕРИАЛЫ И МЕТОДЫ
МАТЕРИАЛЫ И МЕТОДЫ
Скаффолд изготавливали из нетканого материала толщиной около 100 мкм, полученного методом электроспиннинга из поли-L-лактида (ИВС РАН, Санкт-Петербург). Из готового пористого материала вырезали диски диаметром 5 мм, стерилизовали в 70 % этиловом спирте, трижды промывали в фосфатно-солевом буфере и помещали в культуральную среду (DMEM, 10 % фетальной бычей сыворотки). Фибробласты выделяли из биоптата кожи с холки морской свинки по стандартной методике [7]. Культивирование проводили в ростовой среде DMEM с добавлением 10 % фетальной бычей сыворотки. На 2-3 пассаже готовили клеточную суспензию и вносили на подготовленные диски. Через двое суток инкубации дисков из нетканого материала с клетками проводили аутологичную имплантацию на место перфорации БП, затем тампонировали гемостатической губкой согласно стандартной методике. В качестве контроля в другое ухо каждому экспериментальному животному после нанесения перфорации имплантировали аналогично подготовленный образец из нетканого материала без клеток.
Рис.2
Fig. 2.
Visualization of cells in the thickness of the porous scaffold when stained with a fluorescent dye: a – cells attached to the fibers, incr. x 60; b – distribution of cells across the thickness of the carrier.
Результаты гистологического исследования тканей БП показывают локализацию клеток фибробластной морфологии на срезе тканей барабанной перепонки (с одной стороны) (рис. 3), а также прорастание кровеносными сосудами, что говорит о регенерации тканей после имплантации.
а – скаффолд из полилактида с клетками;
б – контроль.
б – контроль.
ЗАКЛЮЧЕНИЕ
ЗАКЛЮЧЕНИЕ
УЧАСТИЕ АВТОРОВ
УЧАСТИЕ АВТОРОВ
Вклад каждого автора. В. С. Шевелева, А. А. Кокорина, А.Е. Голованов – разработка общей концепции и дизайна исследования, анализ данных, написание статьи; Л.А. Мякошина, Н.В. Белый – сбор материалов для исследования, анализ данных; В.Е. Юдин, М.М. Испагиев – анализ данных, подготовка статьи к публикации.
КОНФЛИКТ ИНТЕРЕСОВ
КОНФЛИКТ ИНТЕРЕСОВ
The authors declared no conflicts of interests.
ЛИТЕРАТУРА
ЛИТЕРАТУРА
2.Knutsson J., Bagger-Sjö bä ck D., Von Unge M. Collagen type distribution in the healthy human tympanic membrane // Otol Neurotol. 2009. Vol. 30, No. 12 P. 25-29. doi: 10.1097/MAO.0b013e3181c0e621
3.Volandri G., Di Puccio F., Forte P, Carmignani C. Biomechanics of the tympanic membrane // J. Biomech. 2011. Vol. 44, No. 12. P. 19-36. doi: 10.1016/j.jbiomech.2010.12.023
4.Плужников М.С., Дискаленко В.В., Курмашова Л.М. Современное состояние проблемы хирургической реабилитации больных с хроническими воспалительными заболеваниями среднего уха // Вестник оториноларингологии. 2006. T. 5. С. 63-66. doi: 10.21518/2079-701X-2022-16-23-349-356
5.Sainsbury E., Amaral R.D., Blayney A.W., Walsh R.M., O'Brien F.J., O'Leary C. Tissue engineering and regenerative medicine strategies for the repair of tympanic membrane perforations // Biomater Biosyst. 2022. Vol. 6. doi: 10.1016/j.bbiosy.2022.100046
6.Свистушкин В.М., Тимашев П.С., Золотова А.В., Мокоян Ж.Т. Тканеинженерный подход к закрытию стойких перфораций барабанной перепонки // Медицинский Совет. 2019. Т. 8, С. 132-136. doi: 10.21518/2079-701X-2019-8-132-136
7.Freshney R.I. Culture of animal cells: A manual of basic technique and specialized applications. 6th ed. Hoboken New Jersey: John Wiley & Sons, 2010. 676 p. doi: 10.1002/9780470649367
МИКРОНИЗИРОВАННЫЙ НОСИТЕЛЬ ИЗ ВНЕКЛЕТОЧНОГО МАТРИКСА ПУПОВИНЫ ЧЕЛОВЕКА ДЛЯ 3D КУЛЬТИВИРОВАНИЯ КЛЕТОК
МИКРОНИЗИРОВАННЫЙ НОСИТЕЛЬ ИЗ ВНЕКЛЕТОЧНОГО МАТРИКСА ПУПОВИНЫ ЧЕЛОВЕКА ДЛЯ 3D КУЛЬТИВИРОВАНИЯ КЛЕТОК
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
1Военно-медицинская академия имени С.М. Кирова, Санкт-Петербург, Российская Федерация
2Институт цитологии РАН, Санкт-Петербург, Российская Федерация
журнал "Клиническая патофизиология" № 4 2024г.
Результаты исследований показали, что присутствие микронизированной формы матрикса при культивировании клеток кожи мини-пига положительно влияло на скорость потребления клетками кислорода. Использование микронизированной формы матрикса для культивирования сфероидов из клеток Вартонова студня пуповины человека продемонстрировало активное вовлечение волокон матрикса в сферы и увеличение их объема. Микроноситель обеспечивает большую поверхность для прикрепления клеток и имитирует их микроокружение. Применение матрикса пуповины, создающего оптимальные условия для функционирования клеток, перспективно для разработки бесклеточных изделий для лечения ран и ожогов, инъекционных препаратов для терапии дегенеративно-дистрофических процессов хрящевой ткани, и содержащих клетки тканеинженерных конструкций.
Ключевые слова: микронизированная форма матрикса из пуповины человека, клеточная тканеинженерная конструкция, клеточное дыхание, сфероиды.
MICRONIZED SCAFFOLD FROM HUMAN UMBRICAL CORD EXTRACELLULAR MATRIX FOR 3D CELL CULTURE
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
A.A. Kondratenko1, B.A. Zakopaiko2, D.V. Tovpeko1, S.V. Chebotarev1, S.A. Alexandrova2, P.A. Slizhov1, L.I. Kalyuzhnaya1
1Military Medical Academy named after S.M. Kirov, Saint-Petersburg, Russia
2Institute of Cytology RAS, Saint-Petersburg, Russia
The results. The research results showed that the presence of a micronized form of the matrix during the cultivation of mini-pig skin cells had a positive effect on the rate of oxygen consumption by the cells. Using of the matrix-micronized form for the cultivation of spheroids from Wharton's umbilical jelly cells demonstrated the active involvement of fiber matrices into the spheres and an increase in their volume. The microcarrier provides a large surface area for cell attachment and mimics their microenvironment. Umbilical cord matrix creates optimal conditions for the cell functioning, it is promising for the development of acellular products for the treatment of wounds and burns, injectable remediums for the treatment of cartilage tissue degenerative processes, and tissue-engineered structures containing cells.
Keywords: micronized form of human umbilical cord matrix, cellular tissue engineered structure, cellular respiration, spheroids.
ВВЕДЕНИЕ
Применяемый для формирования ТИК/КИК биополимер должен обеспечивать необходимое микроокружение для клеток, способствуя тем самым их жизнеспособности и стимулированию регенерации тканей invivo. Необходимо, чтобы пространственная организация структуры матрикса обеспечивала беспрепятственный ток жидкостей и питательных веществ. Присутствие в структурных волокнах сигнальных молекул, таких как факторы роста, важно для процессов адгезии, пролиферации и дифференцировки клеток. Постепенная биодеградация имплантируемого матрикса до безопасных продуктов гидролиза, сменяемая появлением внеклеточного матрикса, синтезированного собственными клетками реципиента, завершает восстановление целостности тканей [1].
Разработка матриксов для ТИК/КИК с использованием внеэмбриональных органов представляется одним из наиболее перспективных направлений. Эти аллогенные ткани, лишенные возрастных изменений и влияний внешней среды, утилизируются после родов как биологические отходы. Строма внеэмбриональных органов состоит из различных видов коллагена, содержит большое количество несульфатированных и сульфатированных гликозаминогликанов, фибронектин и многочисленные факторы роста [1]. Другой областью применения матрикса пуповины могут быть клеточные технологии для увеличения популяции, выживаемости клеток.
МАТЕРИАЛЫ И МЕТОДЫ
МАТЕРИАЛЫ И МЕТОДЫ
Эксперимент 1. Первичную культуру получали из кожи мини-пига. Культивировали с добавлением «М» в концентрации 10 мг/мл 21 сутки и исследовали в тесте Seahorse Mito (4 × 103 клеток/лунку; Agilent Seahorse XF, Agilent Technologies, США). В качестве контроля использовали культуру, культивированную в стандартных условиях. Измеряли скорость потребления кислорода (OCR), а также скорость производства протонов (ECAR) в режиме реального времени в течение 90 мин. Анализатор последовательно вводит разобщители и ингибиторы дыхательной цепи и измеряет интенсивность OCR. Олигомицин (ингибитор АТФ-синтазы, блокирует протонный канал необходимый для окислительного фосфорилирования и синтеза АТФ из АДФ и как следствие снижает OCR). FCCP (Карбонилцианид 4-(трифторметокси)фенилгидразон) является разобщителем окислительного фосфорилирования митохондрий, нарушает синтез АТФ, транспортирует протоны через внутреннюю мембрану митохондрий, тем самым усиливает потребление кислорода митохондриями, что приводит к повышению OCR до максимального уровня. Ротенон блокирует перенос электронов на убихинон, тем самым подавляет электрон-транспортную цепь митохондрий. Антимицин А ингибирует восстановление убихинона. Ротенон и антимицин А добавляются совместно, полностью останавливают клеточное дыхание, тем самым снижая OCR до минимального значения.
Эксперимент 2. Клетки Вартонова студня пуповины человека получены в центре коллективного пользования «Коллекция культур клеток позвоночных» Институт цитологии РАН. Для формирования сфероидов использовали 5000 клеток в питательной среде, содержащей «М» 10 мг/мл. В качестве контроля использовали стандартную питательную среду. Через 28 суток культивирования гистологические препараты окрашивали гематоксилином и эозином, по Массону (Biovitrum, Россия), а также исследовали методом сканирующей электронной микроскопии Merlin (Carl Zeiss, Германия).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Рис.1
Скорость потребления кислорода (OCR) и скорость производства протонов (ECAR) клетками, культивированными с использованием микронизированного матрикса из пуповины человека и в контроле
Рис.2
ЗАКЛЮЧЕНИЕ
ЗАКЛЮЧЕНИЕ
ЛИТЕРАТУРА
ЛИТЕРАТУРА
2.Shou Y, Liu L, Liu Q, Le Z, Lee KL, Li H, Li X, Koh DZ, Wang Y, Liu TM, Yang Z, Lim CT, Cheung C, Tay A. Mechano-responsive hydrogel for direct stem cell manufacturing to therapy. Bioactive Materials. 2023 Jun;24:387-400. DOI: 10.1016/j.bioactmat.2022.12.019. PMID: 36632503; PMCID: PMC9817177.
3.Rybkowska P, Radoszkiewicz K, Kawalec M, Dymkowska D, Zabłocka B, Zabłocki K, Sarnowska A. The Metabolic Changes between Monolayer (2D) and Three-Dimensional (3D) Culture Conditions in Human Mesenchymal Stem/Stromal Cells Derived from Adipose Tissue. Cells. 2023 Jan 1;12(1):178. doi: 10.3390/cells12010178. PMID: 36611971; PMCID: PMC9818744.
4.Kouroupis D, Correa D. Increased Mesenchymal Stem Cell Functionalization in Three-Dimensional Manufacturing Settings for Enhanced Therapeutic Applications. Front Bioeng Biotechnol. 2021 Feb 12;9:621748. doi: 10.3389/fbioe.2021.621748. PMID: 33644016; PMCID: PMC7907607.
5.Zhou Z, Xun J, Wu C, Ji C, Ji S, Shu F, Wang Y, Chen H, Zheng Y, Xiao S. Acceleration of burn wound healing by micronized amniotic membrane seeded with umbilical cord-derived mesenchymal stem cells. Mater Today Bio. 2023 Jun 7;20:100686. doi: 10.1016/j.mtbio.2023.100686. PMID: 37334186; PMCID: PMC10276167.
6.Kim JY, Rhim WK, Cha SG, Woo J, Lee JY, Park CG, Han DK. Bolstering the secretion and bioactivities of umbilical cord MSC-derived extracellular vesicles with 3D culture and priming in chemically defined media. Nano Converg. 2022 Dec 19;9(1):57. doi: 10.1186/s40580-022-00349-z. PMID: 36534191; PMCID: PMC9761620.
7.Mawji I, Roberts EL, Dang T, Abraham B, Kallos MS. Challenges and opportunities in downstream separation processes for mesenchymal stromal cells cultured in microcarrier-based stirred suspension bioreactors. Biotechnol Bioeng. 2022 Nov;119(11):3062-3078. doi: 10.1002/bit.28210. Epub 2022 Aug 26. PMID: 35962467.
ПРИМЕНЕНИЕ АНТИМИКРОБНОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ В ХИРУРГИЧЕСКОЙ ПРАКТИКЕ
ПРИМЕНЕНИЕ АНТИМИКРОБНОЙ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ В ХИРУРГИЧЕСКОЙ ПРАКТИКЕ
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
А. А. Глушков¹, К.А. Лебедев¹
1Военно-медицинская академия им. С. М. Кирова, г. Санкт-Петербургжурнал "Клиническая патофизиология" № 4 2024г.
Ключевые слова: антимикробная фотодинамическая терапия, раневой процесс, антибиотикорезистентность.
ANTIMICROBIAL PHOTODYNAMIC THERAPY IN SURGICAL PRACTICEA.
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
S.M. Kirov Military medical academy, St. Petersburg, Russian Federation
Keywords: antimicrobial photodynamic therapy, wound process, antibiotic resistance
ВВЕДЕНИЕ
МАТЕРИАЛЫ И МЕТОДЫ
МАТЕРИАЛЫ И МЕТОДЫ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
У пациентов с применением АФДТ уровень обсемененности ран ниже «критического уровня» был достигнут на пятые сутки, очищение ран, появление грануляционной ткани и начало эпителизации были отмечены на 5,2, 4,8 и 5,8 сутки после начала лечения, в то время как у пациентов, лечение которых не включало АФДТ, уровень обсемененности ран снизился только на 10-15 сутки, а сроки очищения ран, появления грануляций и начало эпителизации были отмечены на 10,5, 9,7 и 11,5 сутки соответственно, что почти вдвое превышает показатели при применении метода АФДТ.
В исследовании Lin и соавт. было представлено применение АФДТ у трех пациентов с инфицированными хроническими язвами нижних конечностей различной этиологии [5]. У всех пациентов проводилось лечение более одного года без эффекта, ввиду чего было принято решение о применении метода АФДТ с использованием 2% раствора 5-аминолевулиновой кислоты. Протокол проведения подразумевал экспозицию раствора фотосенсибилизатора в течение 6 часов с закрытием язвы пластырем с фольгой для предотвращения попадания света и последующего облучения красным светом с плотностью световой дозы 20 Дж/см2 в течение 16,7 минут.
Первый пациент с сахарным диабетом, артериальной гипертензией и двухсторонней полной окклюзией передней большеберцовой и тыльной артерии стопы имел трофическую язву на латеральной лодыжке правой нижней конечности размерами 5х6 см. По результатам посева из раны было высеяно большое количество Enterococcus faecalis. После первого сеанса АФДТ посев из раны уже показал отсутствие роста патогенной микрофлоры. Через 8 месяцев было отмечено заживление 50% язвы, а через 21 месяц – ее полное заживление. В течение 32 месяцев наблюдения не было отмечено рецидива образования язв.
Второй пациент имел трофическую язву правой нижней конечности размерами 6х2 см после комбинированного лечения (хирургическое иссечение язвы и лучевая терапия) плоскоклеточного рака кожи, обсемененную большим количеством Morganella morganii. Отсутствие роста патогенной флоры и появление грануляционной ткани было отмечено после первого сеанса АФДТ. Через 1 и 3 месяца были проведены повторные сеансы, и через 12 месяцев было отмечено полное заживление язвы, при этом в течение 30 месяцев наблюдения не было отмечено рецидивов язвы.
Третий пациент с хронической венозной недостаточностью имел 2 язвы левой нижней конечности: выше и ниже коленного сустава. Верхняя язва была подвергнута только облучением красным светом и послужила контролем, в то время как нижняя язва была обработана 5-аминолевулиновой кислоты с последующим облучением по методике, описанной выше. Авторы отметили, что язва, подвергнутая АФДТ, полностью зажила в течение одного месяца, в то время как контрольная язва оставалась без динамики к 46-му дню наблюдения, после чего была подвергнута АФДТ и полностью зажила через 6 недель. В обеих язвах был отмечен рост S. aureus и P. аeruginosa в начале исследования, причем в обоих случаях после первого сеанса АФДТ не было выявлено роста патогенной микрофлоры.
Авторами был сделан вывод, что АФДТ с использованием 5-аминолевулиновой кислоты не только оказывает выраженный антибактериальный эффект, но и улучшает течение раневого процесса.
Эффективность АФДТ в лечении инфицированных трофических язв было также показано в исследовании Lei и соавт., в которое были включены 26 пациентов с трофическими язвами нижних конечностей, не поддающихся лечению в течение 3 месяцев и инфицированными P. Аeruginosa [6]. 13 пациентам было проведена АФДТ с использованием 20% водного раствора 5-аминолевулиновой кислоты с экспозицией 1,5 часа и облучением светом длиной волны 630 нм и плотностью светового пучка 80 Дж/см2. Остальные пациенты были подвергнуты облучению светом без использования фотосенсибилизатора.
В группе пациентов без применения АФДТ уровень обсемененности ран различался незначительно (5,5 х 107 КОЕ/см2 до и 3,4 х 107 КОЕ/см2 после лечения), в то время как у пациентов, подвергнутых АФДТ через 24 часа после начала лечения, уровень обсемененности ран значительно снизился с 8,9 х 107 КОЕ/см2 до 6,3 х 107 КОЕ/см2 после лечения. Также было отмечено, что площадь раны у пациентов, подвергнутых только облучению светом, уменьшилась с 11,85 до 7,8 см2, а в группе пациентов, получивших АФДТ, уменьшение площади раны было зафиксировано с 12,72 см2 до 3,4 см2.
В работе Бадалова и соавт. был проведен анализ эффективности АФДТ в лечении инфекционных осложнений боевой травмы [7]. В исследование было включено 40 пациентов, которым была проведена АФДТ водным раствором хлорина е6 и облучением красным светом длиной волны 660 нм в течение 7 минут. У 21% больных был выявлен полимикробный пейзаж, в начале лечения уровень обсемененности составлял 2,9 х 106 КОЕ, средняя площадь ран составляла 21,5 см2.
После начала лечения уровень обсеменённости ран снизился до 1,5 х 104 КОЕ на 5-9 сутки, а площадь раневых дефектов уменьшился в два раза в среднем на 13 сутки. Было выявлено, что на 5 сутки после начала лечения происходило значительное уменьшение экссудации и количества гнойного отделяемого, на 9-14 сутки – практически полное очищение ран от отложений фибрина, к 16 суткам – выраженная краевая эпителизация раневых дефектов. Коллективом авторов был сделан вывод, что применение АФДТ в лечении боевой хирургической травмы укоряет переход между 2 и 3 фазами раневого процесса и позволяет улучшить результаты лечения и последующей реабилитации и восстановительного лечения раненых.
Одним из факторов, замедляющих интеграцию метода в широкую клиническую практику, является большое количество различающихся между собой протоколов применения тех или иных фотосенсибилизаторов при различных состояниях. В отсутствие единой базы всех вариантов проведения АФДТ, включая описание используемого фотосенсибилизатора, его концентрации, количества, длины волны, мощности и плотности светового воздействия, практикующему врачу почти невозможно выбрать нужную комбинацию необходимых параметров для достижения наилучшего результата.
Возможным способом систематизации данных наиболее эффективных протоколов может быть использование специальных программ для ведения медицинской статистики, которые способствовали бы более слаженному взаимодействию научно-исследовательской и клинически-прикладной деятельности. В свою очередь, собранные подобным программным способом данные по лечению инфекционных осложнений различных состояний позволят провести автоматизированную эпидемиологическую оценку заболеваемости исследуемыми группами нозологий и распространенности определенных видов инфекций и даст возможность прогнозировать и контролировать распространение полирезистентной флоры [8].
Подобные мероприятия могут быть решением вопроса преодоления низкой эффективности современной антибактериальной терапии и в лучшую сторону повлиять на уровень заболеваемости и качества лечения инфекционных заболеваний хирургического профиля, вызванных резистентной флорой [9]. Также использование данного метода может способствовать улучшению взаимодействия врачей разных специальностей, что не только положительно скажется на самом пациенте, но и может служить основой мультидисциплинарного подхода, который, в свою очередь, также будет способствовать улучшению результатов лечения гнойных осложнений различных терапевтических заболеваний [10].
ЗАКЛЮЧЕНИЕ
ЗАКЛЮЧЕНИЕ
ЛИТЕРАТУРА
ЛИТЕРАТУРА
2.Yan E. et al. Antimicrobial Photodynamic Therapy for the Remote Eradication of Bacteria //ChemPlusChem. 2023. Т. 88. №. 3. С. e202300009.
3.Mahmoudi H. et al. Antimicrobial photodynamic therapy: modern technology in the treatment of wound infections in patients with burns //Journal of Wound Care. 2023. Т. 32. №. 4. С. 31-38.
4.Раджабов А. А. и др. Антибактериальная фотодинамическая терапия гнойных ран мягких тканей //Лазерная медицина. 2017. Т. 21. №. 2. С. 46-49.
5.Lin M. H. et al. Enhancing wound healing in recalcitrant leg ulcers with aminolevulinic acid-mediated antimicrobial photodynamic therapy //Photodiagnosis and Photodynamic Therapy. 2021. Т. 33. С. 102149.
6.Lei X. et al. A clinical study of photodynamic therapy for chronic skin ulcers in lower limbs infected with Pseudomonas aeruginosa //Archives of dermatological research. 2015. Т. 307. С. 49-55.
7.Бадалов В. И. и др. Новые возможности в лечении раневых дефектов при инфекционных осложнениях боевой травмы с использованием антимикробной фотодинамической терапии и рациональным применением антибактериальных препаратов // Журнал инфектологии. 2024. Т. 16. №. 2. С. 17-22.
8.Кузин А. А., Емельянов В. Н., Губанов А. П. и др. Новое программное обеспечение для эпидемиологического мониторинга заболеваемости военнослужащих курсантов // Вестник Российской Военно-медицинской академии. 2018. № S1. С. 92-93.
9.Чеверев В. А., Емельянов В. Н., Киркитадзе Г. Д. и др. Разработка программно-аппаратного устройства для системы мониторинга в телемедицине // Ученые записки УлГУ. Серия: Математика и информационные технологии. 2021. № 2. С. 75-81.
10.Емельянов В. Н., Кузин А. А., Губанов А. П. Использование медико-экономического подхода в оценке социально-эпидемиологической значимости болезней органов дыхания // Эпидемиология и вакцинопрофилактика. 2019. Т. 18, № 1. С. 74-76. DOI 10.31631/2073-3046-2019-18-1-74-76.
ИСПОЛЬЗОВАНИЕ ГЕНЕТИЧЕСКОГО ПАСПОРТА ПРИ ОТБОРЕ ДЛЯ СЛУЖБЫ В АРКТИЧЕСКОМ РЕГИОНЕ
ИСПОЛЬЗОВАНИЕ ГЕНЕТИЧЕСКОГО ПАСПОРТА ПРИ ОТБОРЕ ДЛЯ СЛУЖБЫ В АРКТИЧЕСКОМ РЕГИОНЕ
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
Рубцов Юрий Евгеньевич, к.м.н., ст. преподаватель кафедры ВПТ
Бунтовская Александра Сергеевна, врач клд, НИО МБИ НИЦ
Лобанова Майя Ивановна, член комитета отдела (военно-научного) Военно-научного комитета ГВМУ МО РФ
Глушаков Руслан Иванович, д.б.н., начальник НИО МБИ НИЦ
журнал "Клиническая патофизиология" № 4 2024г.
ВВЕДЕНИЕ
Возможность организма реагировать на «северный стресс» является генетически обусловленной. Эти данные приводятся в многочисленных работах, посвященных генетическим особенностям автохтонных народов Севера.
Таким образом, необходимость генетического паспорта военнослужащего особенно актуальна для тех, кто служит в высоких широтах.
МАТЕРИАЛЫ И МЕТОДЫ
МАТЕРИАЛЫ И МЕТОДЫ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
ACTN3 холодоустойчивость. Наиболее значимым полиморфизмом данного гена является замена нуклеотида C на T в 577 положении – R577X (rs1815739), что приводит к появлению терминаторного кодона и обрыву цепи
BDNF Однонуклеотидный полиморфизм в гене BDNF (Val66Met) регулирует зависимую от активности секрецию нейротрофического фактора головного мозга (BDNF), который влияет на нейропротекцию и синаптическую пластичность.
HTR2A Однонуклеотидная замена Т (тимин) на С (цитозин) располагается в первом экзоне гена HTR2A в положении 102 (rs6313). Данный полиморфизм связан с уровнем экспрессии гена и является маркером психических расстройств. Около 30 исследований показали, что С-аллель является фактором риска развития шизофрении, а также что его частота повышается у людей с алкогольной зависимостью, предрасположенностью к курению, риском возникновения ревматоидного артрита, носители С-аллеля менее агрессивны и более подвержены депрессиям, в то время как у гомозигот TT агрессивность значительно выше Однонуклеотидная замена Т (тимин) на С (цитозин) располагается в первом экзоне гена HTR2A в положении 102 (rs6313). Данный полиморфизм связан с уровнем экспрессии гена и является маркером психических расстройств. Около 30 исследований показали, что С-аллель является фактором риска развития шизофрении, а также что его частота повышается у людей с алкогольной зависимостью, предрасположенностью к курению, риском возникновения ревматоидного артрита, носители С-аллеля менее агрессивны и более подвержены депрессиям, в то время как у гомозигот TT агрессивность значительно выше
LIPC Ген печеночной липазы, LIPC, находится на хромосоме 15q21. Пациенты с полным дефицитом фермента, имеют повышенный уровень общего холестерина и триглицеридов. Мета-анализ, включающий 24 000 человек, для оценки вклада полиморфизма rs1800588 (также известный как C-514T), показал, что носительство минорного аллеля, приводило к повышению ЛПВП на 1,5 мг/дл при генотипе СТ и 3,5 мг/дл при генотипе ТТ (норма — выше 50мг/дл). Таким образом, “Т” аллель являлся протективным в отношении риска развития атеросклероза
FADS1 Белок, кодируемый геном FADS1, является членом семейства генов десатуразы жирных кислот (FADS). Слабый генотип ассоциирован с коронарной недостаточностью и диабетом
MCAD Дефицит среднецепочечной ацил-КоА-дегидрогеназы (MCAD) является наиболее распространенным дефектом бета-окисления митохондрий у людей.
SCAD Вариант 625G>A короткоцепочечной ацил-КоА-дегидрогеназы (SCAD) обусловливает восприимчивость к развитию «клинического дефицита SCAD» и, по-видимому, распространен среди населения в целом.
HIF1A, также HIF-1α — фактор, индуцируемый гипоксией 1-альфа, белок, является субъединицей гетеродимерного фактора транскрипции, фактора, индуцируемого гипоксией 1 (rs11549465), риск ишемического инсульта
eNOS Полиморфизмы гена eNOS являются факторами риска, которые способствуют эндотелиальной дисфункции и атеросклерозу при многих сердечно-сосудистых заболеваниях. Полиморфизмы в экзоне 7 (894 G→ T) и в промоторной области (T-786→C) гена eNOS связаны с функциональными изменениями эндотелия и толщины интимы-медиа сонных артерий, низкой модуляцией предрасположенности к аневризме брюшной аорты и могут быть фактором риска ангиографической ИБС и недавний инфаркт миокарда.
DRD2, Полиморфизм DRD2-141C Ins/Del – отсутствие (делеция) нуклеотида С, расположен в промотере гена – участке, регулирующем транскрипцию, и является функциональным: аллель Del снижает активность промотера, что приводит к снижению уровня экспрессии гена и содержания белка рецептора DRD2
DRD3 полиморфизм rs6280 гена DRD3. Ген DRD3 кодирует дофаминовый рецептор 3-го типа, локализуется в 3-й хромосоме (бэнд q13.3). Аллель C кодирует аминокислоту глицин, аллель T — серин . Данный рецептор рассматривается в качестве гена-кандидата в связи с его ролью в дофаминергической нейротрансмиссии. Функциональная роль полиморфизма связана с изменением афинности рецептора к дофамину и внутриклеточного проведения сигнала. Также у пациентов было обнаружено увеличение плотности DRD3 в области полосатого тела, накопление «усеченных форм» рецепторного белка, образующегося во время альтернативного сплайсинга.
Полиморфизм rs4680 гена COMT был выбран в качестве второго маркера. Ген COMT кодирует катехол-о-метилтрансферазу, локализуется в 22-й хромосоме (бэнд q11.21). Аллель G кодирует валин, аллель A — метионин Данный фермент играет ключевую роль в метаболизме катехоламинов, к которым относятся дофамин, норадреналин. С полиморфизмом rs4680 связана активность фермента, которая определяет уровень концентрации дофамина при передаче сигнала. Кроме того, для европеодиной расы показан повышенный риск развития шизофрении в рамках аддитивной и рецессивной моделей.
VKORC1 rs 9923231 и VDR , связанные с процессами свертываемости крови.
Полиморфные варианты генов выявлялись наборами реагентов для определения полиморфизмов методом ПЦР в режиме реального времени (Синтол, РФ). Анализ результатов генотипирования распределялся на три типа: аллель 1, гетерозигота, аллель 2. Генотипирование образцов геномной ДНК исследуемых образцов проводилось в режиме реального времени на амплификаторе (RT-PCR) ДТ-Прайм (ДНК-Технология, РФ).
Распределение всех исследованных генотипов, как в основной, так и в контрольной группах не различались по критерию Пирсона и соответствовали распределению Харди-Вайнберга. Данные представлены в таблице 1.
ЗАКЛЮЧЕНИЕ
ЗАКЛЮЧЕНИЕ
Для генов общего обмена продолжается процесс их сопоставления с заболеваниями ССС и ЖКТ, манифестирующими при дезадаптации.
ЛИТЕРАТУРА
ЛИТЕРАТУРА
- Воевода М.И. Современные проблемы северной медицины и усилия учёных по их решению / М.И. Воевода, В.И. Хаснулин, Ю.П. Никитин // В кн.: Здоровье коренногго и пришлого населения Чукотского автономного округа. – Новосибирск, 2018. – С. 208–214.
- Пряничников С.В. Функциональное и психофизиологическое состояние работников трудоспособного возраста в Мурманской области // Проблемы сохранения здоровья и обеспечения санитарно-эпидемиологического благополучия населения в Арктике: материалы IV международной научно-практической конференции / под ред. д.м.н. Р.В. Бузинова, д.м.н. Фроловой. – СПб.: Издательско-полиграфическая компания «Коста», 2023. – С. 206–211.
- Фролова Н.А. Мониторинг влияния факторов среды на экологически зависимые заболевания / Н.А. Фролова, И.Ю. Резниченко, А.В. Помозова В.А [и др.] // Проблемы региональной экологии. – 2018. – Т. 3. – С. 19–21.
- Самойлова, И.Ю. Заболеваемость гриппом и острыми респираторными вирусными инфекциями в Якутии во время эпидемических сезонов / И.Ю. Самойлова, С.И. Семенов, М.В. Игнатьева, С.С. Шадрина // Журнал инфектологии. – 2018. – Т. 10, № 1. – С. 103–112.
- Воевода М.И. Современный взгляд на проблему артериальной гипертензии в приполярных и арктических регионах / М.И. Воевода, В.И. Хаснулин // В кн.: Здоровье коренногго и пришлого населения Чукотского автономного округа. – Новосибирск, 2018. – С. 323–331.
- Спивак Д.Л., Шаповалов П.А., Трандина А.Е., Тимошенко Р.В., Захарчук А.Г., Спивак И.М. Психологические ресурсы долголетия и их генетические корреляты. Science and world. 2022. № 11 (111):67-71.
- Лемещенко А. В., Бурлов Н. Н., Гурская О. Е., Спивак И. М., Жекалов А. Н. Полиморфные варианты гена BDNF (rs6265) и их ассоциация с выраженностью когнитивных дисфункций у военнослужащих // Вестник СурГУ. Медицина. 2022. № 4 (54). С. 54–60. DOI 10.34822/2304-9448-2022-4-54-60.
- Спивак И.М., Жекалов А.Н., Спивак Д.Л., Шаповалов П.А., Тимошенко Р.В., Глушаков Р.И., Головко К.П. Роль полиморфных вариантов гена нейротрофического фактора bdnf в процессах активной адаптации к экстремальным условиям и предполагаемой индивидуальной продолжительности жизни. 2023, Известия Российской военно-медицинской академии т.42, №3, 293-301. DOI: 10.17816/rmmar303662
ПРОФЕССОР М. А. ЛУЩИЦКИЙ – ФЛАГМАН ВОЕННО-МОРСКОЙ ХИРУРГИИ
ПРОФЕССОР М. А. ЛУЩИЦКИЙ – ФЛАГМАН ВОЕННО-МОРСКОЙ ХИРУРГИИ
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
Д. А. Суров, Д. А. Дымников, А. П. Уточкин, И. П. Миннуллин, И. А. Соловьев, В. Р. Гольцов, П. П. Лукьянюк, Н. А. Сизоненко
1Военно-медицинская академия им. С. М. Кирова, г. Санкт-Петербургжурнал "Клиническая патофизиология" № 4 2024г.
Михаил Алексеевич создал свою школу блистательных военно-морских хирургов. Он является автором 146 научных работ, дважды избирался председателем Хирургического общества Пирогова. Под его руководством подготовлено и защищено 7 докторских и 18 кандидатских диссертаций. В 1986г. он ушел в отставку. Умер Михаил Алексеевич 10 марта 1999г., похоронен на Богословском кладбище Санкт-Петербурга.
Ключевые слова: морская медицина, кафедра военно-морской и госпитальной хирургии, Лущицкий Михаил Алексеевич, комбинированные поражения, школа военно-морских хирургов.

Родился Михаил Алексеевич в деревне Коловка Минской области в семье сельского почтальона (Рис.2). После окончания средней школы в 1936г. он поступил в 1-й Ленинградский медицинский институт им. И.П. Павлова. С третьего курса он увлёкся хирургией и этот выбор определил всю его дальнейшую жизнь. 1938 год был знаменательным для 1ЛМИ, именно тогда из лучших студентов был образован военно-морской факультет. Судьба распорядилась так, что среди них оказался и третьекурсник М.А. Лущицкий. В 1940г. военно-морской факультет был преобразован в Военно-морскую медицинскую академию, которая, просуществовав 16лет, затем вошла в состав Военно-медицинской академии [1, с. 57].
25 июня 1941г. на выпускном курсе Военно-морской медицинской академии были прерваны государственные экзамены и 222 врача получили назначения на действующие флоты и флотилии. Михаила Алексеевича распределили на Тихоокеанский флот. За участие в боевых действиях с милитаристской Японией Михаил Алексеевич был награжден орденом Красной Звезды (Рис. 3).

на собственные силы [2, с.4], [3, с.108].
После войны в 1948г. М.А. Лущицкий поступил на лечебно-профилактический факультета Военно-морской медицинской академии по специальности «хирургия». После его окончания с отличием в 1951г. Михаил Алексеевич был назначен начальником 1-го хирургического отделения и ведущим хирургом Кронштадтского ВМГ. С первых же шагов своей деятельности в новой должности он пришел к выводу, что в деле совершенствования военно-морского хирурга решающую роль играют элементы новаторства. Поэтому во главу угла своего руководства коллективом хирургов поставил изобретательскую и рационализаторскую работу, и за счет этого добился немалых успехов по всем видам деятельности своего подразделения.

1945г.
Оригинальный хирург с нестандартным научным мышлением был замечен начальником кафедры военно-морской хирургии ВММА, генерал-майором медицинской службы, профессором А. А. Бочаровым, который в то время руководил научными работами, выполняемыми и сотрудниками госпиталя (исторический формуляр 35 ВМГ), и приглашен для поступления в адъюнктуру. Он блестяще сдал вступительные экзамены и был зачислен адъюнктом кафедры военно-морской хирургии.
В период с 1958 по 1961г. М. А. Лущицкий, под руководством А.А. Бочарова и Е.В. Смирнова, подготовил кандидатскую диссертацию, посвященную комбинированной холодовой травме. Ученый совет академии, отмечая большую научную ценность диссертации и ее вклад в фундаментальное изучение проблемы, присвоил М. А. Лущицкому степень доктора медицинских наук.
Михаил Алексеевич Лущицкий главный хирург Военно-Морского Флота
В первой фазе наблюдается замедление миграции нейтрофильных гранулоцитов из кровеносных сосудов в рану, снижение в них активности щелочной фосфатазы, играющей важную роль в фагоцитозе. Во второй и третьей фазах наблюдается более позднее увеличение количества фибробластов в ране, что свидетельствует о замедленном созревании грануляционной ткани. В переохлажденном в воде организме тормозится и эпителизация ран.
Под руководством М. А. Лущицкого был разработан и апробирован в реальных условиях способ лечения переохлажденных в воде раненых, заключающийся в суховоздушном согревании, сочетающимся, после выведения пострадавших из состояния общего глубокого охлаждения, с оксигенобаротерапией и цитохром С-терапией.
В ряде научных работ было показано, что воздействие на организм таких факторов как общее глубокое охлаждение, СВЧ-поле отрицательно влияют на иммунобиологическую резистентность и тормозят заживление ран. В своих выступлениях на научно-практических конференциях выдающийся военно-морской хирург профессор М.А. Лущицкий завещал нам всегда уделять особое внимание теме комбинированных поражений на ВМФ и помнить, что этот вид боевой травмы в современной войне будет преобладать в структуре санитарных потерь как на суше, так и на море (Рис. 5).
Михаил Алексеевич Лущицкий способ лечения переохлажденных в воде
Во главу угла учебного процесса М. А. Лущицкий ставил боевую хирургическую травму, характерную для специфических условий действия сил ВМФ [5, с. 15].
Война в Афганистане, необходимость обобщать опыт лечения современных огнестрельных и взрывных ранений также определили тематику научных исследований кафедры. А. М. Беляев и К. К. Лежнев изучали патоморфологию и кислородный баланс тканей в зоне огнестрельной раны (кандидатские диссертации). Д. М. Суровикин представил рекомендации по использованию новых технологий в лечении огнестрельных ран мягких тканей. И. П. Миннуллин определил показания и противопоказания для ГБО в комплексном лечении огнестрельных ранений. Оба защитили докторские диссертации. В своей кандидатской диссертации С. А. Тетдоев разработал рекомендации по применению специальных устройств для коррекции центральной гемодинамики при внутренних кровотечениях на догоспитальных этапах эвакуации.
Продолжалась разработка клинических тем. Часть работ была выполнена в тесном содружестве с Институтом физиологии АН СССР имени академика И. П. Павлова. Преподаватель кафедры, доцент, полковник медицинской службы В. А. Попов защитил докторскую диссертацию на тему: «Ферментные расстройства при перитоните и их коррекция в комплексном лечении». Этой же теме посвящена его монография. Закончил свои исследования и обобщил их в докторской диссертации «Хроническая дуоденальная непроходимость» доцент А. Д. Слобожанкин.
Большим вкладом в хирургию повреждений явились докторские диссертации преподавателей кафедры М. В. Гринева, Н. Н. Гурина, посвященные патогенезу и лечению огнестрельного остеомиелита и ложных суставов мышечной пластикой и применением аппаратов внеочагового остеосинтеза.
Существенный вклад в развитие идей Е. В. Смирнова о сущности желчнокаменной болезни внес в своих исследованиях преподаватель кафедры подполковник медицинской службы В. А. Тарасов. Полковник медицинской службы Д. М. Суровикин в 1988 г. защитил докторскую диссертацию на актуальную тему о новых рациональных методах лечения гнойных ран. Многолетние исследования кафедры по проблеме миастении обобщил и защитил кандидатскую диссертацию подполковник медицинской службы Г. А. Макиенко; подполковник медицинской службы А. С. Богданов закончил исследования и защитил кандидатскую диссертацию о лечении осложненных форм варикозной болезни. Успешно развивалось направление хирургического лечения щитовидной железы (Л.Ф.Винник, В.С. Зенкин).
Кафедра продолжала разрабатывать ряд прикладных научных тем, имеющих большое значение для нужд флота. Полковник медицинской службы В.Ф. Озеров защитил докторскую диссертацию о возможностях применения на кораблях и подводных лодках вычислительной техники для диагностики острых хирургических заболеваний органов брюшной полости в дальних походах (программа «Медикон»). В 1987 г. вышло в свет руководство М. А. Лущицкого и В. Ф. Озерова «Диагностика и лечение острых хирургических заболеваний органов брюшной полости на кораблях в море с применением ЭВМ».
Очень поучительны и интересны были утренние врачебные конференции и обходы больных, которые проводил Михаил Алексеевич. Они были не только для слушателей источником ценных профессиональных знаний, но и имели большое воспитательное значение, прививая любовь к Флоту, к профессии военно-морского врача, укрепляли высокое чувство долга и преданности Родине. Были случаи, когда Михаил Алексеевич встречался со слушателями и после учебных занятий, передавал им свой богатый опыт службы на Флоте [6, с. 95].
Михаил Алексеевич Лущицкий — автор 146 научных работ, дважды избирался председателем Хирургического общества Пирогова. Под его руководством подготовлено и защищено 7 докторских и 18 кандидатских диссертаций. В 1986 г., в возрасте 67 лет, Михаил Алексеевич ушел в отставку, но не терял связи с кафедрой, активно следил за судьбой своих учеников, работал консультантом крупных лечебных учреждений [7, с.69].
Умер Михаил Алексеевич 10 марта 1999г., похоронен на Богословском кладбище Санкт-Петербурга.
Кафедра бережно хранит в своём музее память о генерал-майоре медицинской службы, профессоре Михаиле Алексеевиче Лущицком. Каждый год в «День памяти ушедших поколений» сотрудниками кафедры проводится траурно-торжественный митинг у могил на Богословском кладбище, где покоятся выдающиеся военно-морские хирурги, в их числе и генерал-майор медицинской службы, профессор Михаил Алексеевич Лущицкий.
КОНФЛИКТ ИНТЕРЕСОВ
КОНФЛИКТ ИНТЕРЕСОВ
The authors declared no conflicts of interests.
ЛИТЕРАТУРА
ЛИТЕРАТУРА
2. Беляев A.M., Озеров В.Ф., Уточкин А.П. и др. К 90-летию генерал-майора медицинской службы профессора Михаила Алексеевича Лущицкого //Всероссийская научно-практическая конференция, посвященная 90-летию профессора М. А. Лущицкого. 2009. С. 3-6.
3. Никитин E.A., Роскостов M.B., Соловьев И.А. и др. Кронштадтский военно-морской госпиталь. 300-лет со дня основания. СПб.: OОO ПДО, 2018. 200 с.
4. Соловьев И.А., Рухляда H.B., Уточкин А.П. и др. М.А. Лущицкий — основоположник учения о комбинированных поражениях в военно-морской хирургии //Сборник материалов научно-практической конференции, посвященной 300-летию 1-го Военно-морского госпиталя. 2015. С. 89-90.
5. Соловьев И.А., Уточкин А.П., Колунов A.B. 80 лет кафедре военно-морской хирургии. СПб.: МОРСАР АВ, 2018. 151 с.
6. Соловьев И.А., Уточкин А.П., Рухляда H.B. и др. Генерал-майор медицинской службы, профессор М.А. Лущицкий - воспитанник кронштадтской школы военно-морских хирургов // Материалы научно-практической конференции, посвященной 300-летию со дня основания Кронштадтского Военно-морского госпиталя. 2017. С. 95- 96.
7. Уточкин А.П., Смирнов С.И. M.A. Лущицкий — выдающийся военно-морской хирург, ученый, педагог // Вестник Российской военно-медицинской академии. 2007. Приложение № 4 (24). С. 69.
ОБЛАДАЕТ ЛИ ТРЕОНИН ПЕЛЛАГРОГЕННЫМ ДЕЙСТВИЕМ?
ОБЛАДАЕТ ЛИ ТРЕОНИН ПЕЛЛАГРОГЕННЫМ ДЕЙСТВИЕМ?
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
журнал "Клиническая патофизиология" № 4 2024г. аланин, кинурениназа, ниацин, 3-оксиантраниловая кислота, пеллагра, треонин, триптофан
Ключевые слова: аланин, кинурениназа, ниацин, 3-оксиантраниловая кислота, пеллагра, треонин, триптофан
DOES THREONINE POSSESS ANY PELLAGROGENIC ACTION?
ИСТОРИЯ СТАНОВЛЕНИЯ ЖУРНАЛА «КЛИНИЧЕСКАЯ ПАТОФИЗИОЛОГИЯ» (к 20-летию от начала издания)
Special design technological bureau «Biofizpribor», St. Petersburg branch of the Federal State Unitary Enterprise «Experimental- production workshops» of Federal Biomedical Agency
Alanine, kynureninase, niacin; 3-oxyanthranilic acid, pellagra, threonine, tryptophan
In 1951 the Soviet biochemist E. V. Gorychenkova demonstrated in her experiments that the majority of amino acids including threonine caused retardation of the kynureninase reaction. Since then the problem of pellagrogenic action of threonine has never been investigated any more either in mammals or in human beings. On the other hand it is known that it is precisely threonine which presents the amino acid whose transformation in the human being differs from its metabolism in animals. In the list of literature given after the paper the pellagrogenic action of threonine redundancy in man is being investigated on the biochemical level.
Keywords: Alanine, kynureninase, niacin; 3-oxyanthranilic acid, pellagra, threonine, tryptophan
ВВЕДЕНИЕ Триптофан, расщепление треонина, треонинальдолаза, треониндегидратаза, лактатдегидрогеназа
Общеизвестно, что наиболее частой причиной пеллагры является однообразное питание кукурузой, ибо в последней отсутствует не только ниацин, но и способный в него превращаться триптофан. Например, молоко бедно ниацином, но богато триптофаном и потому может излечивать пеллагру. Если даже рацион не обеспечивает потребность организма в триптофане и ниацине, триптофан может освобождаться из белков тела и превращаться в ниацин. Однако при одностороннем питании кукурузой этого не происходит. Поэтому до доклада Е.В.Горяченковой [1] (см. ниже) получила подтверждение «токсическая теория», объясняющая возникновение пеллагры поступлением в организм содержащихся в кукурузе токсических веществ ( по Вуллей, цитируемом Горячевой, структурных аналогов и антагонистов ниацина). А именно, стало известно, что добавление к пищевому рациону белков, бедных триптофаном, или отдельных аминокислот-глицина, треонина, фенилаланина, гистидина, задерживает образование ниацина из триптофана.
В 1951 году советский биохимик Е.В.Горяченкова выступила с докладом на сессии АН СССР «Торможение действия кинурениназы аминокислотами и значение его для патогенеза пеллагры». В докладе было сказано, что наличие в составе кинурениназы ПФ, группа которого легко конденсируется с различными аминокислотами в шиффовы основания, приводит к блокированию действия кинурениназы, что объясняет задержку образования ниацина, вызываемую неполноценными белками, в частности, зеином кукурузы. В докладе также сообщалось об опыте, в котором исследовалось влияние аминокислот на расщепление кинуренина (он так же расщепляется кинурениназой, как и образующийся из него в организме 3-оксикинуренин) при инкубировании с ферментной вытяжкой из печени крыс. Только глицин, аспарагин, аспарагиновая кислота и глутаминовая кислота не влияли на величины расщепления кинуренина. Все остальные аминокислоты вызывали торможение кинурениназной реакции. причем некоторые из них, например, треонин, обладали выраженным тормозящим эффектом. Это принципиальный момент, поскольку катаболизм треонина у человека отличается от такового у млекопитающих. Поэтому возникает закономерный вопрос: можно ли по пеллагрогенному действию треонина у крыс судить о пеллагрогенном действии треонина у человека? Причем вопрос о пеллагрогенном действии треонина никогда больше не изучался ни у млекопитающих, ни и у человека: подавляющее большинство исследований после доклада Горячевой вплоть до наших дней было проведено по пеллагрогенному действию избытка другой незаменимой аминокислоты - лейцина, который в большом количестве содержался в пищевом рационе больных пеллагрой. В то же время Горяченкова не выделяет пеллагрогенное действие лейцина: из незаменимых аминокислот она выделила не лейцин, а метионин, фенилаланин, треонин и валин, а также гистидин, заменимый для человека, но незаменимый для крыс [2]. При этом в дальнейшем выводы некоторых исследователей противоречили докладу Горяченковой: лейцин не обладает пеллагрогенным действием; лейцин обладает пеллагрогенным действием, но оно объясняется вовсе не торможением действия кинурениназы; добавление в пищу валина-гомолога лейцина снижает пеллагрогенное действие последнего. Но в последнее время в работе [3] показано, что добавление к пеллагрогенной (бедной белком и не содержащей ниацина) диете крыс изолейцина и валина не только не устраняет ингибирование лейцином превращения триптофана в ниацин, но и усиливает ингибирующее действие, т.к. изолейцин и валин сами обладают этим действием, что подтверждает тезисы Горяченковой.
Все точки над «i» в отношении пеллагрогенного действия лейцина у человека ставит работа Badawy и др. [4]. В ней показано следующее: главным механизмом пеллагрогенного действия лейцина у человека является ингибирование кинурениназы вследствие дефицита ПФ. Этот дефицит возникает в результате расхода ПФ на переаминирование лейцина, которое является начальной стадией катаболизма этой аминокислоты. Это подтверждает главный посыл Горяченковой: избыток различных аминокислот в питании оказывает тормозящее действие на кинурениназу и тем самым приводит к пеллагре .
Выше было замечено, что вопрос о пеллагрогенном действии треонина никогда больше не изучался ни у млекопитающих, ни у человека: И это при том, что Горяченкова сообщила о значительном торможении треонином кинурениназной реакции у крыс. Использование в опытах кинуренина вместо 3-оксикинуренина не могло повлиять на результаты по крайней мере в отношении треонина, т.к. треонин не способен тормозить окисление кинуренина в 3-оксикинуренин по двум причинам: а) является ациклической аминокислотой, что исключает конкуренцию с ароматическим кинуренином б) не требует для своего катаболизма флавиновых коферментов, необходимых для окисления кинуренина в 3-оксикинуренин.
Но сперва необходимо рассмотреть особенности превращения треонина у млекопитающих и человека.
АКТУАЛЬНОСТЬ
АКТУАЛЬНОСТЬ
ЦЕЛЬ ИССЛЕДОВАНИЯ
ЦЕЛЬ ИССЛЕДОВАНИЯ
ПРЕВРАЩЕНИЕ ТРЕОНИНА У МЛЕКОПИТАЮЩИХ
ПРЕВРАЩЕНИЕ ТРЕОНИНА У МЛЕКОПИТАЮЩИХ

Bird и Nunn [7] были первыми, кто усомнился в этом. Они показали, что активность треонинальдолазы в печени крысы низка и заключили, что альдолаза, хотя и присутствует в печени, не может быть главным ферментом распада треонина.
Взаимопревращение треонина и глицина.
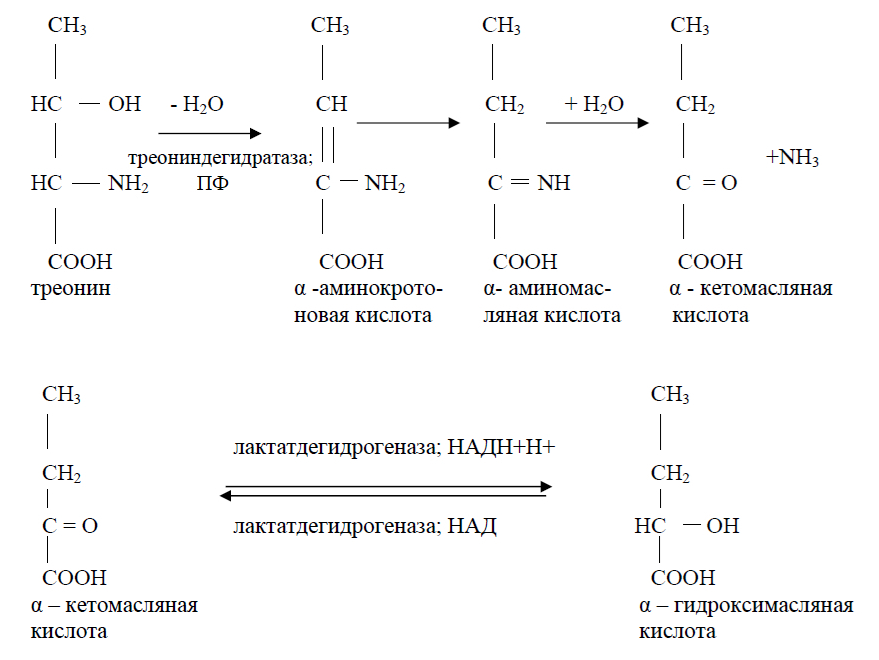
Наиболее убедительное доказательство, свидетельствующее против присутствия реальной «треонинальдолазы» в печени крысы – исчезновение активности треонинальдолазы в цитозольных экстрактах печени нормальных и голодающих крыс, когда треониндегидратаза была устранена имуноосаждением при помощи специфического антитела.
Устранение дегидратазы не воздействует на активность аллотреонинальдолазы (см. ниже).
Необратимый распад треонина с последующим восстановлением α-кетомасляной кислоты.
Дальнейшие исследования подтвердили существование фермента, метаболизирующего аллотреонин (изомер треонина, не входящий в состав белков), возможно, его альдолазы или серингидроксиметилтрансферазы, которые не действуют на треонин [8]. Pagani [9] также подтверждает действие альдолазы именно на аллотреонин, а не на треонин. А в работе Darling и соавторов [10] среди путей катаболизма треонина у взрослых людей треонинальдолаза и вовсе не упоминается. В то же время нет никаких доказательств, что аллотреонин поддерживает рост млекопитающих или встречается как природное вещество, а также, что в печени млекопитающих имеется треонинэпимераза.
Следует также упомянуть серингидроксиметилтрансферазу- пиридоксальзависимый фермент, катализирующий взаимопревращение заменимых аминокислот серина и глицина, широко распространенный в организме млекопитающих. Schrichen и Gross [11] сообщили, что в печени крыс этот фермент идентичен треонинальдодазе. Это послужило установившемуся мнению, что треонин распадается под действием серингидроксиметилтрансферазы. Однако препараты этого фермента, полученные в лабораториях из печени крыс, не проявляли активности треонинальдолазы.. Из этого Ogawa и др. заключили, что у млекопитающих треонинальдолаза отсутствует [12].
Еще в 1974 году академик А.А.Покровский, подчеркивая особую важность для глюконеогенеза у млекопитающих на фоне безуглеводных, богатых белком диет аминокислот серина и треонина (наряду с аланином, аспарагиновой кислотой и орнитином),показал, что за первую стадию их включения в глюконеогенез ответственен фермент сериндегидратаза, который катализирует и реакцию дегидратации треонина, а потому данный фермент может с полным правом быть назван серин-треонин-дегидратазой[13].Значительно позже была установлена идентичность апоферментов(белков)треониндегидратазы и сериндегидратазы[14], а, следовательно, тождественность этих двух ферментов[15 ,16].
Митохондриальный катаболизм треонина заключается в его окислении до α–аминоацетоуксусной кислоты, которая самопроизвольно декарбоксируется, превращаясь в аминоацетон [6] или расщепляется в реакции, катализируемой аминоацетонсинтетазой до глицина и ацетил-КоА [7] (рис.3). Это окисление катализируется НАД-зависимой треониндегидрогеназой и не требует ПФ:

Распад треонина в митохондриях.
ОСОБЕННОСТИ ПРЕВРАЩЕНИЯ ТРЕОНИНА У ЧЕЛОВЕКА
ОСОБЕННОСТИ ПРЕВРАЩЕНИЯ ТРЕОНИНА У ЧЕЛОВЕКА
Edgar [18] приводит сравнение генов треониндегидрогеназы человека и животных и делает вывод, что человек в процессе эволюции утратил способность к синтезу треониндегидрогеназы. треониндегидрогеназы. В [19, 20]. также подтверждают, что у человека из-за генной мутации отсутствует функциональная треониндегидрогеназа. Это позволяет бороться с такими паразитами человека, как трипаносомы, вызывающие сонную болезнь, используя треониндегидрогеназу последних как мишень терапевтического вмешательства. Иными словами, в трипаносомах треониндегидрогеназа является важным для метаболизма ферментом: его ингибирование широким рядом сульфгидрольных реагентов приводит к потере жизнеспособности трипаносом без ущерба для человека.
Все это говорит о том, что единственный путь распада углеродного скелета треонина у человека –распад треонина в цитозоле под действием треониндегидратазы, требующий наличия ПФ. Если учесть, что некоторое количество треонина как у млекопитающих, так и у человека катаболизируется подобно всему лейцину путем переаминирования [21-25] с дальнейшим декарбоксилированием α-кетокислоты, то коферментом трансаминазы также является ПФ.
ЗАКЛЮЧЕНИЕ пеллагрогенное действие избытка треонина
ЗАКЛЮЧЕНИЕ пеллагрогенное действие избытка треонина
Нелишним будет добавить, что и кинурениназа, и треонинжегидратаза обе находятся в цитозоле (а трансаминазы еще в митохондриях), что еще больше усиливает их конкуренцию за ПФ. По этой логике у серина-гомолога треонинапеллагрогенное действие никак не будет меньшим, ибо все 6 путей превращения серина требуют ПФ: внутримолекулярное дезаминирование (как у треонина), переаминирование, декарбоксилирование, взаимопревращение с глицином, превращение в цистеин путем пересульфирования с токсичным гомоцистеином с устранением последнего и превращение в аминоспирт сфингозин, входящий в состав сфинголипидов (третье, четвертое, пятое и шестое в животном организме для треонина отсутствует). Да, Горяченкова в своем докладе выделила и серин, но он а) является заменимой аминокислотой и будет все равно синтезироваться в организме даже при полном отсутствии его в пище б) его превращения у человека не отличаются от других животных и что справедливо для крысы, справедливо и для человека. Поэтому пеллагрогенное действие избытка треонина у человека должно учитываться при составлении рационов. О суточной потребности человека в треонине я уже писал[25].
ЛИТЕРАТУРА
ЛИТЕРАТУРА
2.Малиновский А.В. Особенности метаболизма гистидина у разных видов животных // Генетика и разведение животных. 2023. Т.3. P.103-109. https://doi.org/10.31043/2410-2733-2023-3-103-109
3. Shibata К., Taniguchi I., Onodera M. Effect of Adding Branched-chain Amino Acids to a Nicotinic Acid-free, Low-protein Diet on the Conversion Ratio of Tryptophan to Nicotinamide in Rats // Biosci. Biotech. Biochem. 1994. Vol. 58, №5. Р. 970-971. https://doi.org/10.1271/bbb.58.970
4. Badawy A. A-B., Lake S.L., Dougherty D.M. Mechanisms of the Pellagragenic Effect of Leucine: Stimulation of Hepatic Tryptophan Oxidation by Administration of Branched-Chain Amino Acids to Healthy Human Volunteers and the Role of Plasma Free Tryptophan and Total Kynurenines // Int. J. Tryptophan Res. 2014.Vol. 4, №7. Р.23-32. doi: 10.4137/IJTR.S18231. eCollection 2014
5. Дэгли С., Никольсон Д. Метаболические пути / Пер. с англ. М.: Мир, 1973.
6. Neuberger A. Glycine formation from L-threonine // Comp. Biochem. 1981. 19A. Р. 257-303.
7. Bird M.I., Nunn P.B. Measurement of L-threonine aldolase activity in rat liver // Biochem. Soc. Trans. 1979. Vol. 7. P. 1274 – 1276. https://doi.org/10.1042/bst0071274
8. Yeung Y.G. Threonine aldolase is not a genuine enzyme in rat liver // Biochem J.1986. Vol. 237. P. 187–190. .https://doi.org/10.1042/bj2370187
9. Pagani R. L-allothreonine and L-threonine aldolase in rat liver // Biochem. Soc. Trans. 1991.Vol. 19, №3.Р. 3465.
10. Darling P. B., Grunov J., Rafii M., Brookes S., Ball R.O., Pencharz P.B. Threonine dehydrogenase is a minor degratative pathway of threonine catabolism in adult humans // Am. J. Physiol. Endocrinol. Metab. 2000. Vol.278. P. 877-884. doi: 10.1152/ajpendo.2000.278.5.E877
11. Schirch I.,Gross T. Serine transhydroxymethylase Identification as the threonine and allothreonine aldolases // J.Biol.Chem. 1968. Vol. 243. P.5651-5655.
12. Ogawa H., Gomi T.,Fujioka. M. Serine hydroxymethyltransferase and threonine aldolase are they identical? // The International Journal of Biochemistry and Cell Biology.2000.Vol. 32. P. 289 -301. https://doi.org/10.1016/S1357-2725(99)00113-2
13. Покровский А. А. Роль биохимии в развитии науки о питании. Mосква: Наука.1974.
14. Watanabe R., Fujimura, S., Kadowaki, M., Ishibashi, T. Effects of dietary threonine levels on the threonine-degrading enzyme activities and tissue threonine related amino acid concentration in rats // Anim. Sci. Technol. (Jpn.).1998. Vol.69. P.108--116.
15. Housse J.D., Hall B.N.,Brosnan J.T. Threonine metabolism in isolated rat hepatocytes // Am.J. Physiol. Endocrinol.Metab.2002. Vol. 281. Е1300-Е1307. https://doi.org/10.1152/ajpendo.2001.281.6.E1300
16 .Nagao K., Bannai M., Seki S., Mori M., Takahashi M. Adaptational modification of serine and threonine metabolism in the liver to essential amino acid deficiency in rats // Amino Acids.2009. March. https://doi.org/10.1007/s00726-008-0117-7
17. Zhao X.H., Wen Z.M., Meredith C.N., Matthews D.E., Bier D.M., Young V.R. Threoninekinetics at graded threonine intakes in young men //Am. J. Cln. Nutr. 1986. Vol. 43.P. 795-798. https://doi.org/10.1093/ajcn/43.5.795
18. Edgar A.J. The human L-threonine-3-dehydrogenase gene is an expressed pseudogene // BMC Biochem.2002; Vol.3, №18.Р1-13. https://doi.org/10.1186/1471-2156-3-18
19. Chuanchin H.,Hao G.,Jiaxu W.,Weiguang L.,Yide M.,Mian W. Regulation of L-threonine dehydrogenase in somatic cell reprogramming // Stem.Cells.2013. Vol.31.P.953-965. https://doi.org/10.1002/stem.1335
20. Winkle L.J.V.,Gallet V.,Iannaccone P.M. Threonine appears to be essential for proliferation of human as well as mouse embryonic stem cells // Cells and developmental biology. 2014. Vol.2, №18. Р 18. https://doi.org/10.3389/fcell.2014.00018
21. Idle J. R., Seipel K., Bacher U.,Pabst T.,Beyoglu D. (2R,3S)-Dihydroxybutanoic Acid Synthesis as a Novel Metabolic Function of Mutant Isocitrate Dehydrogenase 1 and 2 in Acute Myeloid Leukemia // Cancers (Basel). 2020. Vol. 12, №1. Р. 2842. doi: 10.3390/cancers12102842.
22. Малиновский А.В. Открытия японских биохимиков, ломающие традиционные представления о превращении треонина и гистидина в организме человека и значение этих открытий в лечении уремии // Клиническая нефрология. 2021.Т.13, №3. С.54-58. Doi: https://dx.doi.org/10.18565/nephrology.2021.3.00-00
23. Малиновский А.В. Незаменимые аминокислоты и их α-кето- и гидроксианалоги в диете больных уремией (биохимический аспект) // Клиническая нефрология. 2022. Т. 14, № 1. С. 94–101. DOI: 10.18565/nephrology. 2022.1.94-101 34.
24. Малиновский А.В Возможность замещения треонина безазотистыми аналогами в диете больных диабетическими нефропатиями: биохимический аспект // Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова. 2022. Т.14, №3. С.5-12. DOI: https://doi.org/10.17816/mechnikov108652
25. Малиновский А. В. Биохимические причины лимитирующего характера треонина и других незаменимых аминокислот и отсутствия этого характера у некоторых млекопитающих и человека // Клиническая патофизиология. 2023. Т.29, №2. С.33-42.


